Quanto ci tieni alla sicurezza ed integrità dei dati della tua azienda?
Prendo spunto da questo interessante articolo pubblicato su MQ – Magazine Qualità che parla di sicurezza ed integrità dei dati per parlarvi delle funzionalità di QualiWare che potrebbero rispondere alle esigenze che vengono spiegate da Ezio Boiani, senior consultant del Gruppo Galgano.
Per chi non avesse tempo o voglia di leggere l’articolo, il succo è che la sicurezza dei dati è un problema ancora poco sentito dalle persone e di conseguenza dalle aziende anche se entro i prossimi 5 anni il traffico cloud (i contenitori di dati e informazioni in internet) e quello dei data-center (i mega server che fisicamente contengono i dati del cloud) cresceranno di 4 volte. Questo renderà ancora più grande il problema della sicurezza ed integrità dei dati.
Nelle aziende la sicurezza e la riservatezza dei dati, siano essi in cloud o all’interno dei server aziendali, deve diventare uno dei punti cardini delle attività da svolgere.
I dati più sensibili sono ovviamente quelli relativi alle persone, i loro dati anagrafici, i loro contratti e le loro malattie. Ma anche molti documenti aziendali devono essere trattati con altrettanta riservatezza e integrità.
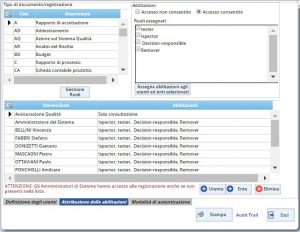
QualiWare permette innanzi tutto di impostare criteri di accesso alle informazioni e ai documenti che consentono di restringere la possibilità di accedere a determinate informazioni e documenti solo a determinate persone. Questo, soprattutto per la parte di gestione delle risorse umane, diventa un punto fondamentale per garantire la riservatezza dei dati.
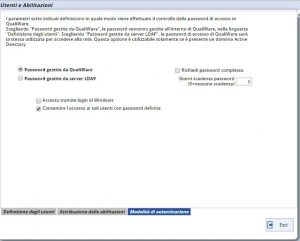
Una delle prime azioni che implementano la sicurezza è l’impostazione di una password complessa e l’obbligo di sostituirla in maniera periodica. Questa impostazione può essere gestita da QualiWare in due maniere distinte: da QualiWare stesso o prendendo le impostazioni del vostro dominio Windows.
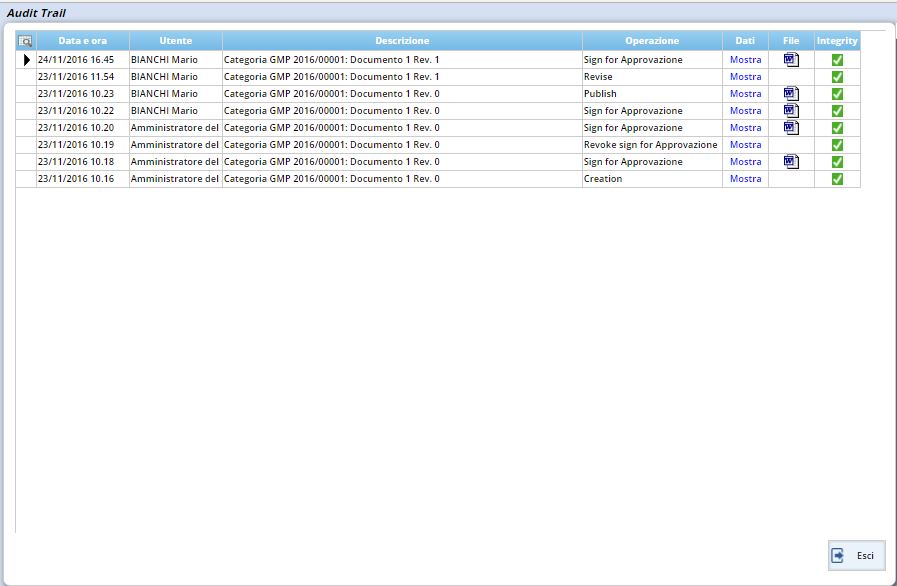
Un’altra funzionalità estremamente importante che garantisce l’integrità dei dati è l’attivazione dell’Audit Trail che consente di mantenere traccia delle modifiche fatte ad un documento e di chi le fa, mantiene una copia del documento prima della modifica e monitora anche tutti i cambiamenti dei diritti di accesso.
Inoltre l’Audit Trail non è modificabile e fa uso della crittografia per rilevare eventuali modifiche indebite effettuate da utenti che accedono direttamente al database tramite strumenti esterni o profili amministrativi ad alto livello.
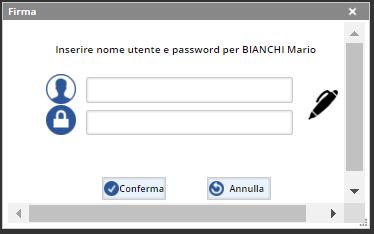
Infine la funzionalità della Firma Forte, cioè la richiesta di nome utente e password prima che si possa effettuare una qualunque modifica o che si possa dare il proprio benestare ad una fase del processo di gestione della documentazione, impediscono che utenti non autorizzati effettuino delle azioni al posto di un’altra persona. Solitamente queste fasi o modifiche possono essere fatte “liberamente”, avendo gli opportuni permessi, una volta che si è effettuato l’accesso al programma con il proprio utente e password.
Queste due ultime funzionalità, cioè l’Audit Trail e la richiesta di nome utente e password ad ogni modifica possono essere attivati in maniera puntuale alle sole categorie documentali che si ritiene che debbano essere protette maggiormente. Questo consente di non appesantire o rallentare il lavoro degli utenti quando devono gestire documenti che non necessitano di un grado così elevato di riservatezza o integrità.
Tutti questi elementi di sicurezza uniti alle funzionalità garantiti dal database che fa da base al programma lo rendono adeguato ad essere utilizzato in un contesto conforme alla norma ISO/IEC 27001:2013.
Queste funzionalità sono state implementate soprattutto per rendere QualiWare validabile secondo le linee guida delle normative Annex 11 EU GMP e dalla 21 CFR Part 11.
QualiWare è quindi il programma adatto non solo a chi vuole gestire in maniera efficace ed efficiente un’azienda certificata ISO 9000 (soprattutto nella nuova versione ISO 9001:2015 basata sulla gestione per processi), ISO 14001 o OHSAS 18001, ma anche a chi deve mantenere e garantire INTEGRITA’, RISERVATEZZA e DISPONIBILITA’ dei dati ai propri utenti e clienti.
Compila il form sotto per avere maggiori informazioni.
Errore: Modulo di contatto non trovato.